Affaires réglementaires
La conformité de vos évaluations cliniques assurée par notre CRO
Votre conformité, assurée par nos services en Affaires Réglementaires.
Nos experts sécurisent vos interactions avec les autorités et vous accompagnent dans la maîtrise de vos essais cliniques et de votre documentation réglementaire, en conformité avec les exigences ICH-GCP, ISO 14155 et 21 CFR Part 11. Nous prenons en charge vos obligations liées au règlement MDR 2017/745 et au règlement IVDR, incluant des activités clés telles que le Clinical Evaluation Report (CER) et le PMCF pour les dispositifs médicaux.
Objectif : zéro surprise, zéro rejet, zéro écart critique.
Nos domaines d’intervention
CRO Affaires réglementaires : une prise en charge complète de vos obligations réglementaires
Nous intervenons sur l’ensemble du périmètre réglementaire afin de garantir la conformité de vos essais sur médicaments et dispositifs médicaux :
Soumissions réglementaires
Clinical Trial Application (CTIS), autorités sanitaires, RA/MOH, IRB, Ethics Committee
Documentation clinique & pharmaceutique
Dossiers IMPD, IB, CEP, PSUR, DSUR, rapport d’évaluation clinique CER, plans et rapports PMCF dispositif médical
Grâce à notre expertise en affaires réglementaires et qualité, nous sécurisons la cohérence et la conformité de votre documentation tout au long du cycle de vie produit.
Affaires réglementaires
Gestion des affaires réglementaires : conformité MDR/IVDR et maîtrise documentaire
Centaur Clinical met à votre disposition une équipe d’experts pour consolider votre dossier technique. Nous assurons la conformité de vos dispositifs médicaux au règlement MDR 2017/745 et au règlement IVDR, la préparation et la mise à jour de votre CER, vos plans et rapports PMCF, ainsi que la coordination de vos essais cliniques. Nous garantissons la maîtrise documentaire (eTMF QC), le suivi qualité, la gestion des CAPA et la préparation aux audits et inspections.
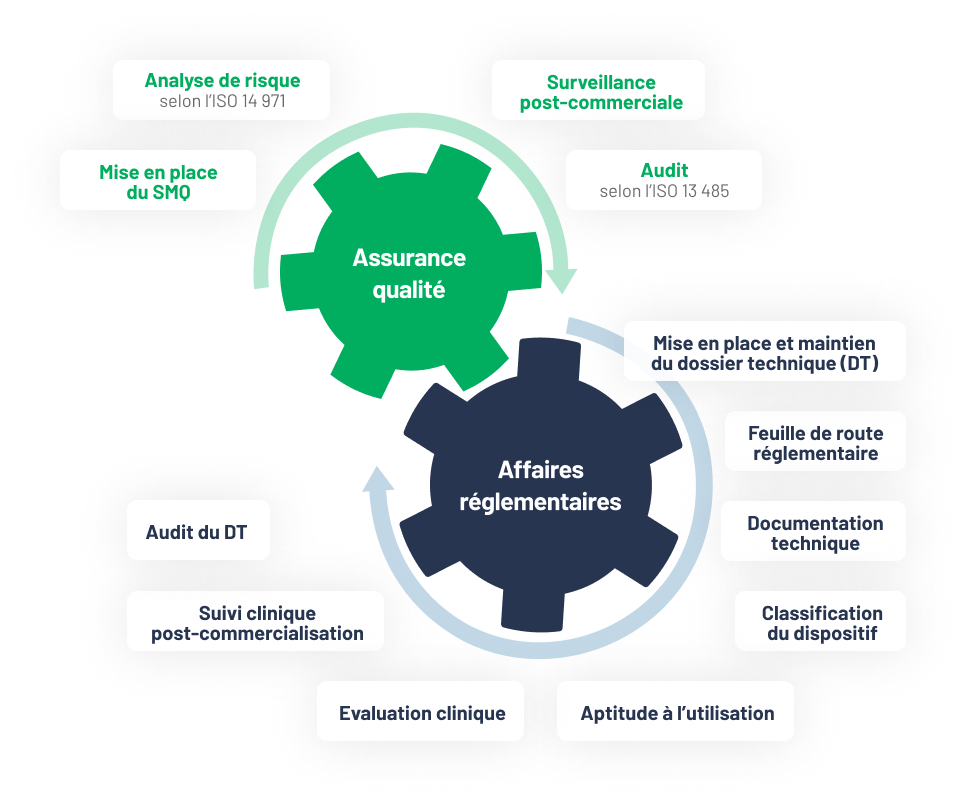
Analyse et stratégie réglementaire
Identification des exigences applicables (MDR/IVDR, pays), analyse des écarts, plan de soumission, stratégie clinique (CER, PMCF) et cartographie documentaire (IMPD, IB, CEP, PSUR/DSUR).
Soumissions et interactions autorités
Préparation des dossiers CTA/CTIS, coordination avec les autorités (RA/MOH) et comités d’éthique, réponses aux questions (Q&A), variations, mises à jour documentaires jusqu’à l’approbation.
J’ai un projet
Centaur Clinical intervient à n’importe quel stade du DT et du SMQ
Nous accompagnons le fabricant pendant le processus de certification CE avec l’organisme notifié.

Témoignages
Nos clients satisfaits parlent de nous
Nous démarrons une investigation clinique avec Centaur Clinical et nous sommes pour l’heure très satisfaits de notre collaboration. La préparation de la soumission aux autorités est une période stressante et chronophage qui mobilise du personnel qualifié. Les équipes de Centaur Clinical ne manquent pas de nous apporter leur expertise, disponibilité et support.

Centaur Clinical nous a aidé à définir un rationnel et une stratégie d’investigation clinique solide et cohérent vis-à-vis des attentes des ON relativement à l’application du RDM et des preuves cliniques nécessaires à apporter.

